近期,放射性诊疗创新药物研发团队在药物化学权威期刊J Med Chem杂志发表背靠背文章,分别介绍了团队在99mTc及18F核素标记的同源及异源成纤维细胞活化蛋白(FAP)靶向探针方面的研究成果,为创新FAP靶向探针工具箱增添了新成员。文章的第一作者分别为博士生孟令欣、方建阳博士及硕士生陈学东。
(1)FAP靶向探针系列之99mTc标记FAPI同源二聚体(Rational Design and Comparison of Novel 99mTc-Labeled FAPI Dimers for Visualization of Multiple Tumor Types)
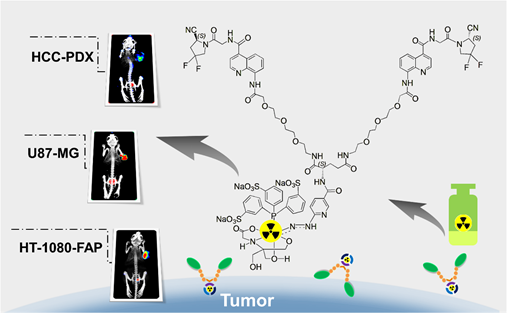
近年来,成纤维细胞活化蛋白(FAP)因其独特的表达使其成为FAP靶向分子成像和放射治疗的有希望的靶点。FAP靶向的PET示踪剂(例如68Ga-FAPI-04和68Ga-FAPI-46)已表现出良好的肿瘤成像能力,并在多个方面具备优于[18F]氟脱氧葡萄糖(FDG)的诊断性能。然而,在FAP靶向的SPECT成像示踪剂研发方面的报道相对较少。考虑到SPECT在核医学中的重要性以及成纤维细胞激活蛋白(FAP)在癌症诊断和治疗中的关键作用,我们将目标聚焦于FAP靶向SPECT成像探针的开发与应用。开发99mTc标记的FAPI示踪剂可丰富SPECT探针工具箱,并大大拓展SPECT成像的应用。二聚化或多聚化已在多个靶点的探针设计中被证明是增强肿瘤摄取和延长药物病灶滞留的有效策略。然而,到目前为止,尚未有99mTc标记的FAPI二聚体被报道。为此,课题组设计并验证了不同99mTc标记策略对FAP靶向二聚体探针SPECT成像性能的影响。

团队成功合成二聚体HF2,搭配各种共配体(tricine、TPPTS、EDDA和TPPMS)通过一锅法及药盒化形式进行99mTc标记,获得不同类型的二聚体探针[99mTc]Tc-TPPTS-HF2、[99mTc]Tc-EDDA-HF2和[99mTc]Tc-TPPMS-HF2。SPECT成像结果表明,[99mTc]Tc-TPPTS-HF2比[99mTc]Tc-EDDA-HF2和[99mTc]Tc-TPPMS-HF2表现出更高的肿瘤摄取和靶/非靶比(T/NT)。值得注意的是,[99mTc]Tc-TPPTS-HF2在HT-1080-FAP和U87-MG荷瘤小鼠中表现出良好的肿瘤积累,该性能显著优于单体[99mTc]Tc-TPPTS-HF。此外,[99mTc]Tc-TPPTS-HF2在肝细胞癌患者来源的异种移植瘤(HCC-PDX)模型中亦呈现良好的成像对比度。
(2)FAP靶向探针系列之18F标记FAPI异源二聚体(Rational Design and Pharmacomodulation of 18F-Labeled Biotin/FAPI-Conjugated Heterodimers)
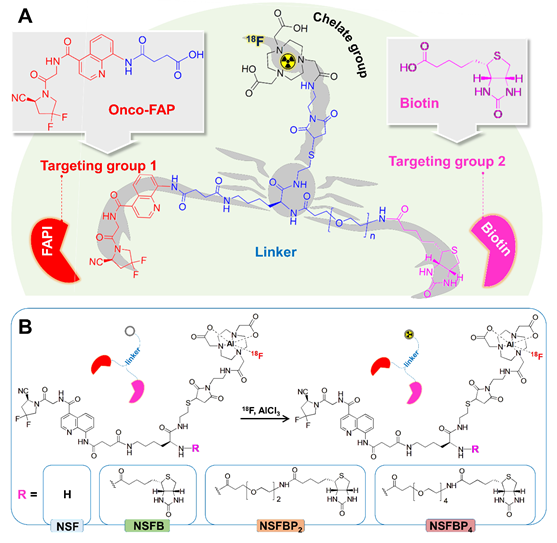
尽管靶向FAP的放射性配体在临床应用中具有重要的前景,但有几个挑战值得考虑:探针肿瘤摄取低及滞留不足等在一定程度上阻碍了放射性标记FAPI 探针的应用,特别是在原发性癌症患者的靶向放射性核素治疗(TRT)或 PET/SPECT 延迟成像中。此外,在TME未完全形成或FAP在CAFs上的表达不足的情况下,阳性肿瘤可能表现出阴性组织区域,从而损害放射性配体的敏感性。目前,与单靶点分子相比,[68Ga]Ga-FAPI-RGD(靶向FAP和整合素αvβ3)和[68Ga]Ga-FAPI-PSMA(靶向FAP和前列腺特异性膜抗原PSMA)在某些适应症中获得更好的效果。可见,具有较长肿瘤保留时间的异源二聚体放射性示踪剂在癌症诊疗中具有非常大的转化潜力。
癌细胞表现出对生物素的高度和快速摄取,以支持其生长和增殖。进一步的研究证实,与正常组织细胞相比,在肺癌、结肠癌等浸润性肿瘤细胞上高水平表达生物素受体BR。与FAP 类似,BR 代表了一种广谱肿瘤靶标,有必要针对这两个泛癌靶点设计新的探针组合。基于上述背景,为了有效应对以上挑战,可以采用具有双受体靶向特性的异源二聚体来增强肿探针的瘤靶向性。本研究设计了一系列具有双受体靶向特性的异源二聚体,能够同时识别FAP和BR。 OncoFAP和生物素可以通过NOTA连接,并用18F-Al标记形成放射性探针[18F]AlF-NSFB、[18F]AlF-NSFBP2和[18F]AlF-NSFBP4。将该类双靶探针与相应的FAP单靶向探针 [18F]AlF-NSF 进行比较,可进一步证实生物素靶向基团对探针性能的促进作用。在四类探针中,[18F]AlF-NSFBP4在肿瘤部位快速且高度富集,肿瘤轮廓清晰,而在包括肝、肺、肠、肌肉等主要器官或组织中均呈现低摄取并被快速清除,可呈现良好的靶/非靶比值。且肿瘤中的摄取具有持久的滞留,在注射后4 h仍然具有高的肿瘤摄取及成像质量。
针对FAP这一重要的肿瘤诊疗靶点,团队及合作单位进行了持续深入的研究,不断创新优化探针结构,已在J Med Chem(3篇)及J Nucl Med(2篇)、 Theranostics(2篇)等高水平期刊发表研究成果。以上研究为丰富团队FAP靶向探针种类提供了重要的拼图,也为创新核素诊疗探针结构提供了借鉴。我中心郭志德老师、北京协和医院张现忠教授,厦门大学附属第一医院李业森博士、中心方建阳博士分别作为以上文章的共同通讯作者。该研究得到了国家自然科学基金、厦门大学南强青年拔尖人才项目等多项基金项目的资助。
文章链接1:https://pubs.acs.org/doi/10.1021/acs.jmedchem.4c00772
文章链接2:https://pubs.acs.org/doi/10.1021/acs.jmedchem.4c00544
文章链接3:https://pubs.acs.org/doi/10.1021/acs.jmedchem.1c02162