肝细胞癌(HCC)的TACE治疗常伴发病灶的转移并受到炎症干扰等限制。冷等离子体(CAP) 作为新兴电离技术则可以实现对肝脏肿瘤的选择性消融,但其仍存在组织渗透性有限的难题。中心博士生李昌红等设计并搭建了柔性微导管冷等离子体(FPM)设备。将传统的金属微针探针转换为可弯曲的非金属微管探针,可将CAP精准输送到深部肿瘤通过以降低组织损伤风险,并显著提高手术精度和安全性。此外,使用环形电极而不是传统的针形电极也可以增加自由基的产生和治疗效率,同时避免意外放电的风险,使治疗更安全、更有针对性。与传统的冷等离子体治疗机制不同,经FPM生成的CAP可屏蔽具有细胞毒性紫外线和臭氧,在细胞层面通过ROS/Caspase-8/GSDMC通路诱导肝细胞癌发生非炎症性细胞焦亡效应。由于Gasdermin-C(GSDMC)在肝细胞癌中高表达,但在正常组织中几乎不表达,这便保证了CAP治疗的选择性靶向性和以及对炎症反应的缓冲。
随后,研究团队将FPM与栓塞材料(EM)-PPP@CD水凝胶相结合。该联合策略既增强了栓塞药物的可注射性,又有助于原位肝癌的栓塞效果和药物的持续释放。结果表明,FPM-EM联合更有效地减小大鼠原位HCC的大小,并促进CD3/CD4/T-helper和CD3/CD8A细胞毒性T细胞在肿瘤区域内的浸润。该策略整合了CAP和栓塞技术的优势,使CAP能够递送到深层组织,同时也解决了TACE的局限性。此FPM-EM联合治疗的策略可显著增强抗肿瘤免疫力,这表明FPM-EM可作为安全、有效和微创的HCC新疗法,并揭示了一种非炎性焦亡机制,同时进一步拓宽了基于CAP的肿瘤治疗的潜力。
该研究通过开发用于精准治疗HCC的FPM装置,提出了CAP与经动脉栓塞介入治疗的创新整合。该联合治疗方案可最大限度地减少炎症,同时增强抗肝癌免疫反应,从而提供更安全、更有效的治疗策略。此外,AI驱动的MRI数据分析也进一步确认了该疗法的精确性和临床适用性。与此同时,FPM-EM平台还有望扩展到其他肿瘤的介入治疗,并适应整合多种药物和纳米/微材料,进而推动临床转化研究。
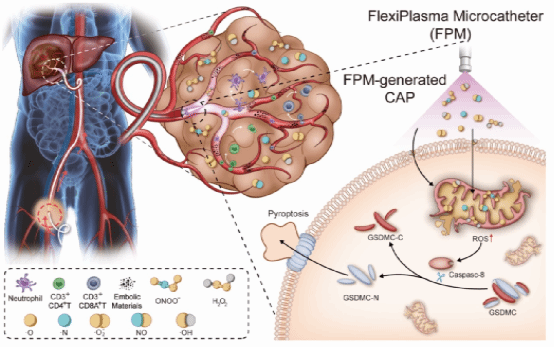
FPM及其在HCC治疗中的应用示意图。
FPM产生CAP并与栓塞材料结合,以实现协同效应。CAP诱导肿瘤微环境中产生RNOS,通过胱天蛋白酶-8介导的GSDMC激活引发焦亡。而栓塞物质有助于血管闭塞,由此联合治疗可联合治疗招募包括中性粒细胞、CD3+CD4+和CD3+CD8A+T细胞,导致免疫激活,进而抑制肝癌的发生发展。
该研究成果《FlexiPlasma Microcatheter-Embolic Material (FPM-EM) Platform: A Non-Inflammatory Pyroptosis Strategy for Precision Hepatocellular Carcinoma Therapy》已发表于《Small Methods》期刊。
论文链接: https://doi.org/10.1002/smtd.202500231

