
近年来,近红外二区(Near-infrared II, NIR-II)成像因具备更深组织穿透与更低背景噪声,被认为是提升术中导航与深部病灶可视化能力的重要方向。然而,在肝胆外科疾病诊疗中,胆道损伤及胆漏作为最严重的并发症之一,往往需要在复杂组织遮挡下实现精准识别。相比之下,传统临床荧光造影剂(如吲哚菁绿 ICG等)主要在 NIR-I 窗口工作,存在穿透深度不足(<2 mm)与空间分辨率受限等瓶颈,制约了其在复杂胆囊及胆道等手术中的进一步应用与胆漏的敏感检测。与此同时,长期严重的胆囊炎、胆汁淤积等疾病以及胆漏等术后并发症可触发局部肝脏炎症反应:在肝组织微环境中,过量活性氧(Reactive Oxygen Species, ROS)与肝星状细胞(Hepatic Stellate Cells, HSCs)异常激活会促进细胞外基质过度沉积,特别是可加速合并肝纤维化甚至肝硬化患者的疾病进展,甚至可能会显著增加其癌变风险。考虑到终末期肝硬化或肝细胞癌的高死亡率风险,如何早期实现上述疾病精准可视化诊断与干预治疗一体化,成为临床上肝胆疾病管理的重要科学问题。
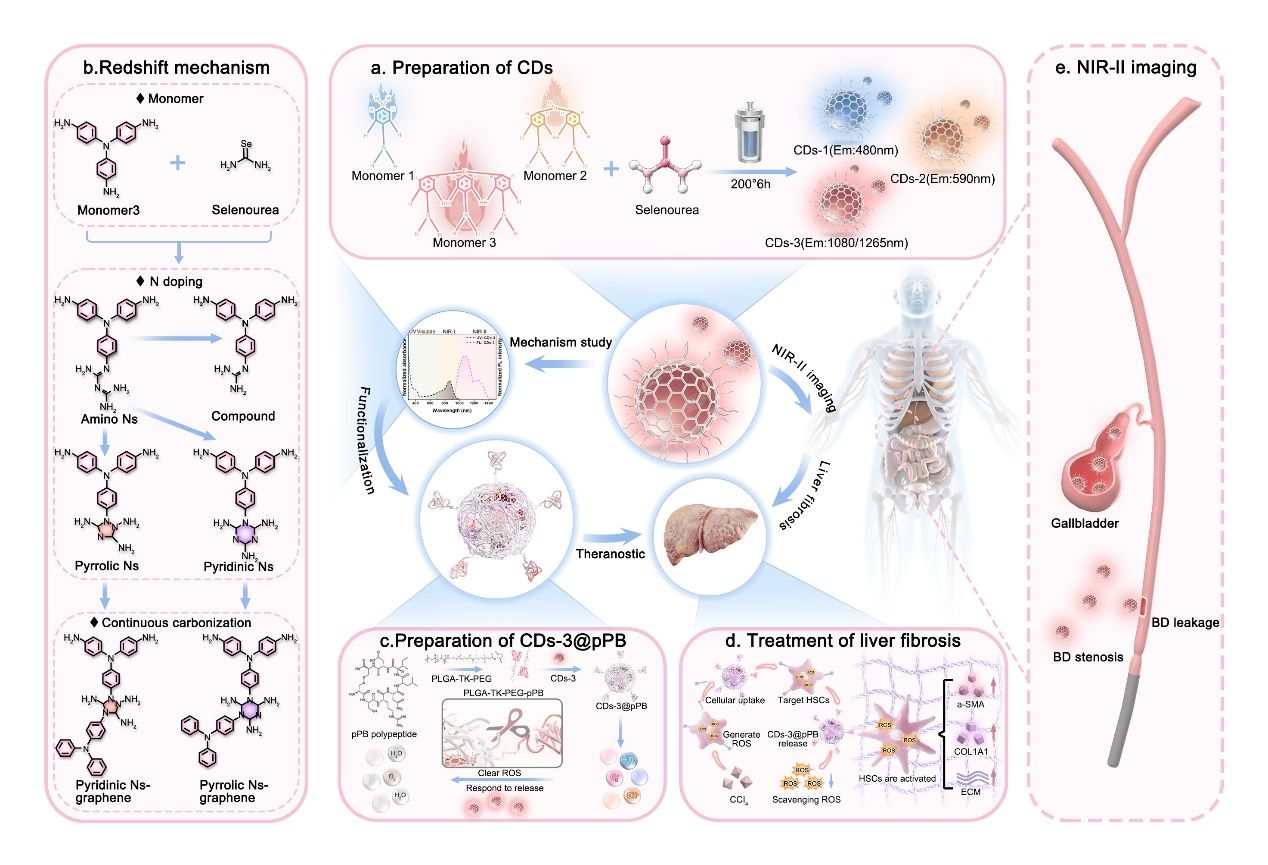
为应对上述挑战,中心博士生阳丽娟在刘刚教授指导下提出一种全新的 NIR-II 碳点(carbon dots, CDs)分子工程策略:以对苯二胺衍生物为前驱体,通过“苯胺结构逐级延伸”构建可控分子骨架,获得发射覆盖 480–1265 nm 的碳点体系,其中 CDs-3 展现出显著的 NIR-II 发光性能,并呈现 1080 nm 与 1265 nm 双峰最大发射。基于 CDs-3 的光学优势,该研究在仿生胆囊疾病模型中实现 808/980 nm 双激发与多通道成像;在组织遮挡条件下,即便覆盖 15 mm 组织仍可获得清晰图像与较高的信噪比,其穿透深度性能显著优于 ICG。鉴于上述优异的表现,团队进一步地构建了功能化复合CDs-3@pPB探针 :该探针通过 PLGA-TK-PEG-pPB 修饰提升肝靶向性与生物相容性,并引入 ROS 响应键(TK)实现炎性微环境智能响应,使其在保持 NIR-II 成像能力的同时兼具 ROS 清除与抑制 HSCs 激活的治疗能力,并在小鼠肝纤维化模型中展现出良好的治疗效果。
总体而言,该研究围绕肝胆系统疾病诊治中“更深的穿透力、更高的分辨率、更低的背景干扰”成像与肝纤维化早期精准干预的临床需求,提出碳点分子工程新策略,构建出可发射至NIR-II的碳点体系,并在此基础上实现了肝胆系统疾病深部高质量成像与肝纤维化诊疗一体化应用,为肝胆疾病的精准成像导航与早期干预治疗提供了具有临床转化潜力的精准化诊疗平台。
近日,该研究成果以“Engineering NIR-II carbon dots through aniline extension with graphene and nitrogen enrichment for hepatobiliary theranostics” 为题在线发表于Nature Communications。中心博士生阳丽娟、李满、彭一晟为论文共同第一作者,中心刘刚教授、药学院陆治香副教授及澳门大学曲松楠教授为论文共同通讯作者。本研究获得国家重点研发计划、国家自然科学基金、翔安创新实验室科技项目资助。
论文链接:https://www.nature.com/articles/s41467-026-70150-7